Questions et réponses avec le Paul Nghiem MD, PhD
 Mark Teich, Directeur Exécutif de ″Skin Cancer Foundation″, s’est entretenu avec Paul Nghiem, MD, PhD, à propos des progrès décisifs dans la détection, la surveillance et le traitement des patients atteints du cancer à cellules de Merkel (CCM), un cancer cutané rare, mais dangereux. Le Dr Nghiem est le Président de la fameuse “George F. Odland Chair″ et dirige le Service de Dermatologie à l’Université de Washington à Seattle. Il est l’un des meilleurs experts du CCM aux USA.
Mark Teich, Directeur Exécutif de ″Skin Cancer Foundation″, s’est entretenu avec Paul Nghiem, MD, PhD, à propos des progrès décisifs dans la détection, la surveillance et le traitement des patients atteints du cancer à cellules de Merkel (CCM), un cancer cutané rare, mais dangereux. Le Dr Nghiem est le Président de la fameuse “George F. Odland Chair″ et dirige le Service de Dermatologie à l’Université de Washington à Seattle. Il est l’un des meilleurs experts du CCM aux USA.
Question : Le mélanome tue plus de patients que toute autre forme de cancer cutané. Mais comme le CCM est beaucoup plus rare que le mélanome, il est plus dangereux, cas pour cas. Pourquoi?
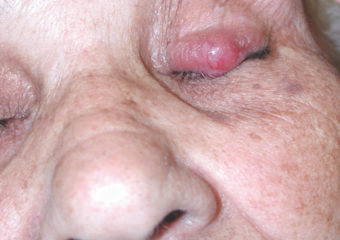
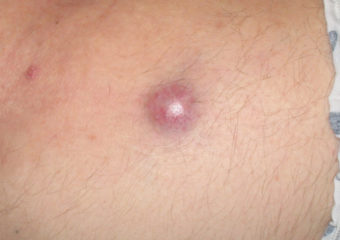
Réponse : Les formes précoces de CCM sont typiquement moins faciles à diagnostiquer que celles de mélanomes récents. Comme elles ne paraissent pas inquiétantes, elles ne sont détectées qu’à un stade plus avancé, quand elles ont déjà métastasé vers d’autres régions. Elles sont alors beaucoup plus difficiles à guérir. Par contre, de nombreux mélanomes sont véritablement diagnostiqués à un stade “in situ” (stade 0) confinés dans les couches superficielles de la peau (épiderme), sans avoir encore gagné les couches profondes. Ces mélanomes in situ sont faciles à traiter et n’ont – en principe – aucune chance de produire des métastases (1% des cas). Par contre, sur plus de 1000 cas de CCM que nous suivons, nous n’en avons observés que 2 avec lésions in situ. Il est donc malheureusement rare de les détecter à ce stade précoce.
Lorsque vous découvrez un mélanome ou un CCM, la crainte initiale réside dans le fait que la tumeur primitive ait déjà envoyé des métastases vers les ganglions lymphatiques les plus proches. La technique standard pour s’en assurer actuellement s’adresse à la biopsie du ganglion sentinelle (BGS). Elle permet de vérifier que les cellules cancéreuses n’ont pas envahi les ganglions lymphatiques après leur examen histopathologique.
Au cours du mélanome, dans la plupart des cas, la tumeur est petite et à un stade suffisamment précoce pour que la recherche du ganglion sentinelle soit limitée vu la faible probabilité d’une telle métastase. Toutefois, même les plus petites CCM (3 ou 4 mm de diamètre) comptabilisent 15% de chances d’avoir envahi le territoire ganglionnaire et/ou au-delà : c’est pourquoi nous estimons indispensable la recherche du ganglion sentinelle même si la CCM est très petite.
Question : Que peut-on faire pour diagnostiquer plus souvent ces lésions à un stade encore curable ? Comment reconnaitre plus précocement des CCMs potentiels?
Réponse : Les signes classiques de l’ABCDE du mélanome ne sont pas adaptables au CCM. Par contre, nous avons proposé un acronyme, AEIOU, qui peut faciliter sa découverte précoce.
A = Asymptomatique/lésion insensible
E = Extension rapide
I = Immunodépression
O = Optimal après 50 ans
U = Ultraviolets (avec expositions du sujet surtout à peau claire)
Environ 63 % des CCM augmentent rapidement et près de 90 % présentent 3 ou 4 des modifications indiquées par l’acronyme. Il est toutefois important de souligner que de nombreuses lésions comportant plusieurs des caractères de l’AEIOU, n’étaient pas des CCM. Certaines étaient bénignes, d’autres témoignaient d’une variété de cancer cutané différente.
Question : Une fois que le CCM a métastasé vers les ganglions lymphatiques ou au-delà, quelles sont les chances de survie du patient?
Réponse: Jadis, nous traitions les formes avancées du CCM par chimiothérapie. Cette technique réduisait les tumeurs dans plus de la moitié des cas, mais le bénéfice obtenu ne dépassait pas 3 mois en moyenne. Quand le cancer récidivait, il devenait résistant à plusieurs cytotoxiques et le système immunitaire était déprimé compliquant les problèmes pour ce qui est véritablement un cancer immuno-sensible. Cependant les inhibiteurs “check point” sont une nouvelle classe imunothérapeutique (traitements qui renforcent les capacités du système immunitaire dans sa lutte contre une maladie). Ils sont rapidement devenus le traitement standard des formes avancées de CCM. En bloquant les récepteurs de protéines qui maintiennent le système immunitaire normalement sous surveillance, ces médicaments stimulent les cellules T pour combattre la tumeur. En 2014, un check point inhibiteur le pembrolizumab (Keytruda) qui bloque une protéine immuno-inhibitrice appelée PD-1 (programmed death-1) a été récemment acceptée pour combattre les mélanomes avancés, offrant de longues rémissions à de nombreux patients. Il est maintenant utilisé à d’autres fins lors d’essais cliniques concernant le CCM. Notons qu’aucune médication n’a encore été approuvée officiellement dans le traitement du CCM par la FDA.
Des investigateurs ont également testé un nouveau “check point blocked”, l’avelumab sur des CCM. Il stimule les cellules T en bloquant une molécule appelée PD-L1 qui travaille avec PD1, pour inhiber ces cellules immunitaires. Différents essais cliniques pour chacune des drogues sont en cours et, en 2015, le statut “fast track” et le “break through therapy” ont été accordés pour accélérer leur développement et leur reconnaissance par le FDA.
Nous pensons que le pembrolizumab et l’avelumab sont susceptibles d’obtenir l’agrément pour le CCM en 2017 car il est clair maintenant que ces drogues sont infiniment plus bénéfiques et moins dangereuses que la chimiothérapie traditionnelle.
Question : Laquelle de ces 2 médications a obtenu les meilleurs résultats?
Réponse : Il est impossible de répondre parce que ces médicaments ont été testés dans différentes populations. Les 2 drogues bloquent le même processus général pour revivifier et stimuler les cellules T, si bien qu’il n’existe pas de différence bien claire en ce qui concerne l’efficacité de ces 2 agents pour le moment.
Question : Y a-t-il un ordre préférentiel dans la prescription des médicaments à l’heure actuelle?
Réponse : Jusqu’à récemment la chimiothérapie venait en tête. Mais si vous traitez des CCM avancés avec un “check point” inhibiteur avant de prescrire la chimiothérapie, environ 60% des malades réagissent favorablement. Si vous attendez l’échec de la chimiothérapie pour traiter les patients avec le check point inhibiteur, seuls 40% répondent bien. Enfin, après 2 ou 3 cycles chimiothérapiques, environ 20% seulement des sujets bénéficient alors du traitement. Par conséquent, l’abord logique semble qu’on utilise en premier lieu le “check point” inhibiteur puis on décide de la conduite à tenir en fonction de la réponse. Certains patients présenteront une “guérison” complète avec rémission totale de la maladie. Certains CCM réagiront partiellement, souvent avec une diminution de 70% du volume de la tumeur, ce qui représente encore une très belle réponse. Mais habituellement, si le médicament doit agir, la réponse thérapeutique est rapide et dans la plupart des cas dépasse bien une année. Toutefois, nous ignorons ce qu’il adviendra si le traitement est stoppé. Bien que la chimiothérapie ne soit plus considérée comme le traitement initial, l’irradiation peut dans certains cas être utilisée avantageusement très tôt. Sa synergie avec l’immunothérapie est indiscutable. Le système immunitaire agit en éliminant plus efficacement les petites tumeurs que les grandes et l’irradiation peut diminuer de façon effective le volume des tumeurs. Si bien que l’on peut irradier les lésions les plus importantes d’abord pour les réduire et diminuer l’importance du cancer avant d’utiliser le traitement “check point blockade”. Le système immunitaire peut alors agir plus efficacement en éliminant les petites tumeurs.
Question : Que sait-on encore à propos des autres traitements” FDA approved-blockade check point” concernant le mélanome comme le nivolumab (Optivo) et l’association Opilimumab (Yervoy)-Nivolumab ? Ont-ils été essayés sur le CCM?
Réponse : Il n’existe pas de publications concernant ces médications à propos du CCM, mais un nouvel essai recrute des patients. Toutefois nous avons déjà vu quelques patients qui ont obtenu d’excellents résultats avec cette association.
“Je me sentais découragé en examinant des patients atteints d’une forme métastatique de CCM. Maintenant, clairement, la situation n’est plus désespérée.”
Question : Que fait-on si aucun de ces traitements n’agit?
Réponse : C’est actuellement un immense sujet d’intérêt et de recherche. L’association de 2 médications immuno-stimulantes de type différent est une zone d’exploration majeure. Il est également possible que des injections locales de thérapies immuno-stimulantes pour éliminer une cible tumorale spécifique puisse être associée à un agent systémique immunothérapique. On peut aussi réaliser une association chimiothérapique ou une irradiation à des traitements bloquant les points de rencontre immunitaires mais de telles combinaisons n’ont pas encore été étudiées et nous ne savons pas si elles sont efficaces.
Question : Vous avez dit que vous vous attendez à ce que la moitié des patients aillent bien lors du traitement bloquant des points de rencontre immunitaires. Cela suggère qu’il existe une moitié des malades n’allant pas mieux. Comme ces traitements sont coûteux avec, pour certains, un sérieux potentiel d’effets secondaires, existe-t-il un moyen de prévoir quels patients seront susceptibles d’en bénéficier afin de débuter un traitement plus efficace pour cette catégorie.
Réponse : Bien que plus de la moitié des patients soient de bons répondeurs, chez environ 40% d’entre eux le cancer continue de progresser comme si on ne leur donnait aucun traitement. Malheureusement nous ne pouvons pas, à l’heure actuelle, prévoir lesquels sont susceptibles de s’améliorer. Nous, et beaucoup d’autres, travaillons d’arrache-pieds pour résoudre ce problème, mais à ce jour, aucun parmi la douzaine de tests que nous avons effectués n’a apporté la solution.
Question : Que peut-on dire après l’administration d’un traitement : y a-t-il un moyen de savoir précocement si le cancer s’apprête à rechuter?
Réponse : Nous avons effectué des travaux excitants dans ce domaine. Notre équipe a développé un test sanguin qui recherche certains anticorps du polyomavirus des cellules de Merkel. Ce test nous permet de détecter rapidement une rechute à un stade où la tumeur pourra être traitée avec plus d’efficacité (www.merkelcell.org/sero). En 2008, Patrick Moore et Yuan Chang ont découvert que la plupart des CCM sont pour une partie d’entre eux causés par un virus (les rayons solaires jouent souvent un rôle également). Nous trouvons ce polyomavirus des cellules de Merkel dans environ 80% des CCM. Lorsque ce virus infecte des cellules il produit des oncoprotéines susceptibles de permettre à ces cellules de croitre anarchiquement. Nous effectuons des tests sanguins à différents intervalles en débutant lors du diagnostic et si le taux des anticorps de ces protéines à polyomavirus continue de s’accroitre, il annonce indubitablement la rechute.
Nous utilisons maintenant ce test de façon régulière parce qu’il est indispensable dans le suivi du patient. Environ la moitié des malades ne produisent aucun de ces anticorps et ils sont en réalité environ 40% dont le risque de rechute est plus élevé que chez ceux qui les fabriquent. Par conséquent nous devons les examiner attentivement en pratiquant des scanners. Chez les patients qui montrent des anticorps, c’est relativement simple : si le cancer ne rechute pas, les anticorps disparaissent rapidement et dans la plupart des cas ils sont indétectables après 1 an de traitement. Si le CCM se manifeste, les anticorps remontent. Cela nous offre de grandes chances de déceler des rechutes précocement à un stade où elles sont facilement traitables (traiter un grain de raisin au lieu d’une grappe – en termes de dimensions du cancer – fait la différence). Enfin, chez un patient dont les anticorps continuent de chuter, les tests sanguins nous confortent en ce qui concerne l’absence de rechute, si bien que nous pouvons échapper à des scans coûteux, ou du moins en réduire la fréquence.
Environ 2 douzaines d’institutions réparties dans les USA utilisent actuellement ces tests et un groupe européen développe un test similaire au nôtre. Nous avons publié la première description de notre test en 2010. Utilisant l’aide apportée par une bourse du NIH, nous avons maintenant suivi plus de 200 CCM nouvellement diagnostiqués pour évaluer l’utilité de ce test. Nos patients et nous-même l’avons trouvé très utile et notre seconde grande étude pour sa validation a paru récemment dans le journal Cancer.
Question : Après que vous ayez traité des CCM, à quel rythme décidez-vous de les revoir et quel est le taux du risque de rechute?
Réponse : Pendant plusieurs années, nous avons eu des données intéressantes sur la durée de survie des patients diagnostiqués à différents stades du CCM, mais c’est récemment seulement que nous avons obtenu des données concernant ceux qui avaient rechuté. A ma grande surprise, elles se sont avérées incroyablement utiles. Par exemple, quand les patients viennent d’être diagnostiqués, vous pouvez leur dire qu’à un stade 3 il existe 70% de chances de rechute tandis qu’un stade I précoce peut n’avoir que 20% de chances de récurrence. Lorsque les patients vous voient à l’occasion de leur visite annuelle, il est maintenant possible de leur dire quelle est l’importance du risque “résiduel” de la maladie en utilisant les données “survie sans rechute” (c.a.d. durée de vie du patient sans rechute). Si la lésion n’a pas rechuté au bout de 3 ans, l’immense risque d’une récurrence a disparu.De plus, il est important de savoir que même en cas de rechute, le stade auquel la tumeur originale a été diagnostiquée joue un rôle important dans sa gravité potentielle. Lorsqu’une rechute apparait chez des sujets diagnostiqués au stade I, ils sont habituellement proches du stade primaire, même avec des ganglions, et ils peuvent être traités avec succès. Par contre, quand des malades diagnostiqués au stade 3 ont une rechute, les métastases apparaissent souvent à distance et sont beaucoup plus dangereuses.
Toutes ces données nous étaient inconnues jusqu’il y a encore quelques mois. Elles ont prouvé leur utilité en permettant d’évaluer plus efficacement les malades. Nous devons probablement les suivre à la lettre et pour de nombreuses années encore… En général, nous pensons, maintenant, que nous n’avons pas à revoir les patients de façon si proche pendant de nombreuses années comme nous le faisions jadis. Le CCM ne parait pas semblable au mélanome qui souvent réapparait 5 ou 10 ans après le diagnostic. Le CCM, s’il rechute, c’est dans les 2 ou 3 ans. Si bien que nous pensons actuellement que le suivi intensif pendant 2 ou 3 ans est tout à fait approprié avec un calendrier infiniment moins rigoureux jusqu’à la 5e année. Ces données ne sont pas encore publiées mais elles sont disponibles sur : https://merkelcell.org/prognosis/disease-recurrence.
Question : Existe-t-il de nouvelles formes différentes de traitement?
Réponse : Le blocage des points de rencontre immunitaires a été le grand tournant, et aucun autre traitement test n’a réalisé cette sorte de différence dans l’évolution de la maladie.
Cependant en association avec le traitement, des points de rencontre immunitaires, nous utilisons maintenant les propres cellules T spécifiques du virus du patient pour combattre le cancer. Dans les CCM induits par les virus, vous pouvez découvrir rapidement ces cellules T, les recueillir, les faire croitre avec des facteurs de croissance qui prolongent leur existence et renforcent leur pouvoir “tueur”, puis on les réinjecte au patient. Ceci peut produire un renforcement du système immunitaire, et la combinaison de ce traitement avec celui du blocage des points de rencontre immunitaires peut être plus efficace que ces thérapeutiques isolées.
Nous cherchons également à associer des traitements intralésionnels avec ceux bloquant les points de rencontre immunitaires. Ce sont des immunothérapies telles que les interférons, l’interleukin-12 ou les agonistes récepteurs du Toll-like qui sont injectés directement dans la tumeur des patients. Dans de courtes études sur le CCM, les traitements intralésionnels ont souvent diminué le volume des tumeurs injectés, voire éliminé et réduit d’autres tumeurs corporelles. Des études sont en cours, mais il semble probable que des simulateurs immunologiques locaux prescrits avec les agents des points de rencontre immunitaires nous permettront d’élever le taux de réponses favorables à un meilleur niveau qu’avec les traitements effectués isolément.